A funkciós csoportok szerepe a molekulák tulajdonságainak meghatározásában
A funkciós csoportok az organikus kémia alapvető építőkövei, amelyek meghatározzák a szerves vegyületek jellemző kémiai és fizikai tulajdonságait. Ezek speciális atomcsoportok, amelyek a szénvázhoz kapcsolódva egyedi reakcióképességet és viselkedést kölcsönöznek a molekuláknak. A téma jelentősége a kémia tudományán belül kiemelkedő, hiszen a szerves kémia alapját a szén és a hozzá kapcsolódó funkciós csoportok adják. Ezek nélkül nem lenne érthető az élővilág kémiai felépítése, a gyógyszerek működése vagy az ipari anyagok előállítása. A funkciós csoportokkal való foglalkozás számtalan hétköznapi és technológiai területen megjelenik - a háztartási tisztítószerek összetételében, az élelmiszeripari adalékanyagokban, az üzemanyagokban, vagy akár a textiliparban.
A funkciós csoportok definíciója és alapvető jelentősége
A funkciós csoport egy speciális atomcsoport a szerves molekulában, amely döntően befolyásolja a vegyület kémiai viselkedését és reakciókészségét. A legegyszerűbb példák közé tartozik a hidroxilcsoport (-OH), az amino-csoport (-NH₂), a karbonilcsoport (-C=O), vagy a karboxilcsoport (-COOH). A szerves vegyületek osztályozása is ezen alapul: például ha a funkciós csoport egy -OH, akkor alkoholról, ha -COOH, akkor karbonsavról beszélünk.
A funkciós csoport jelenléte meghatározza a molekula reakcióit - például, hogy savas, bázikus, könnyen oxidálható, vagy éppen redukálható lesz-e. A szén vázhoz kapcsolódó funkciós csoport mindig meghatározza, hogy a molekula mely részén lesz a kémiai reakciók központja (ún. reaktív centrum). A funkciós csoport jelenléte a molekulában elektronos effektusokat (induktív és mezomer effektus) válthat ki, és befolyásolhatja a szferikus effektusokat, melyek mind hozzájárulnak a vegyület egyedi reaktivitásához. A szén és funkciós csoportok kapcsolata nemcsak a vegyületek szerkezetét, de fizikai jellemzőit is alapvetően befolyásolja: például, hogy a molekula vízoldható lesz, vagy sem, poláros vagy apoláros, illetve milyen halmazállapotú szobahőmérsékleten.
A szénváz, hibridizáció és telítettség hatása
A szénatom egyedülálló képessége, hogy négy kovalens kötéssel bármilyen más atomhoz kapcsolódhat, alapot teremt a funkciós csoportok változatosságának. A szénatom elektronpályáinak átrendeződése, azaz hibridizációja három fő formában jelenik meg a szerves kémiában: sp³, sp² és sp hibridállapotban. Az sp³ hibridizációjú szén például tetraéderes szerkezetet eredményez, mely az alkoholoknál vagy aminoknál a leggyakoribb. Az sp²-es hibridizáció síkháromszög szerkezetet ad, ami a karbonilcsoporttal rendelkező vegyületeknél (pl. aldehidek, ketonok) jellemző. A szénváz telítettsége alapvetően meghatározza, hogy milyen típusú funkciós csoportok kapcsolódhatnak hozzá. Ezzel szemben a telítetlen szénlánc, amely tartalmaz kettős (alkének) vagy hármas kötések (alkinek), különleges reakcióképességet ad.

Különböző funkciós csoportok és jellemzőik
A szerves kémiában számos, eltérő tulajdonságú funkciós csoport létezik. Nézzük meg a legfontosabbakat, és azt, hogy hogyan befolyásolják a molekula tulajdonságait.
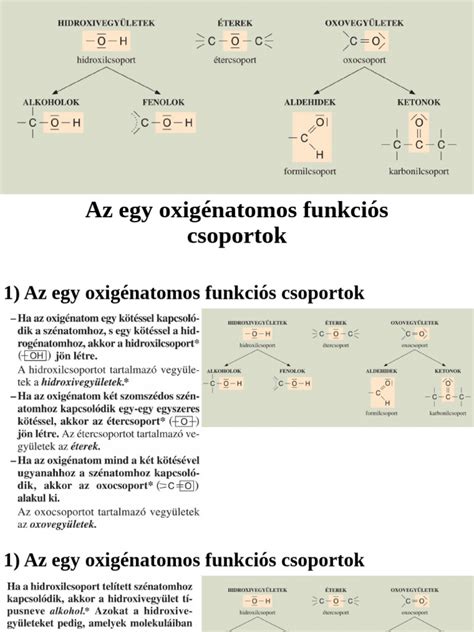
Hidroxilcsoport (-OH)
A hidroxilcsoport (-OH) az egyik legegyszerűbb és leggyakoribb funkciós csoport, amely szénatomhoz kapcsolódik. Az alkoholokban található meg, ahol a szénlánc egyik szénatomjához közvetlenül kapcsolódik. A hidroxilcsoport jelenléte alapvetően megváltoztatja a szénhidrogének tulajdonságait. A nem poláris alkánokhoz képest az alkoholok sokkal polárisabbak, képesek hidrogénkötések kialakítására, ami jelentős hatással van forráspontjukra, olvadáspontjukra és oldhatóságukra. Ezenkívül a hidroxilcsoport reaktív centrumot biztosít, amely lehetővé teszi az alkoholok számára, hogy számos kémiai reakcióban vegyenek részt, mint például oxidáció, dehidratáció, észterezés vagy nukleofil szubsztitúció.
Az alkoholok osztályozása az -OH csoporthoz kapcsolódó szénatom jellege alapján történik:
- Primer (elsődleges): Ha az -OH csoporthoz kapcsolódó szénatomhoz csak egy másik szénatom kapcsolódik.
- Szekunder (másodlagos): Ha az -OH csoporthoz kapcsolódó szénatomhoz két másik szénatom kapcsolódik.
- Tercier (harmadlagos): Ha az -OH csoporthoz kapcsolódó szénatomhoz három másik szénatom kapcsolódik.
Ez az osztályozás rendkívül fontos, mivel befolyásolja az alkoholok reakciókészségét, különösen az oxidációs reakciók és a nukleofil szubsztitúciós mechanizmusok szempontjából. A hidroxilcsoport térbeli elhelyezkedése is meghatározó. Az oxigénatom sp3 hibridizált, és a kötésszögek közel 109,5 fokosak, hasonlóan a vízmolekulához vagy az éterekhez.

Karbonilcsoport (C=O)
A karbonilcsoport (C=O) két fő típusa az aldehidekben és a ketonokban fordul elő. Az aldehidek esetében a karbonilcsoport a lánc végén található, míg a ketonokban két szénatom között helyezkedik el. Például a formaldehid (HCHO) egyszerű aldehid, míg az aceton (CH₃COCH₃) a legismertebb keton. Az sp²-es hibridizáció síkháromszög szerkezetet ad, ami a karbonilcsoporttal rendelkező vegyületeknél jellemző.
The carbon cycle - Nathaniel Manning
Karboxilcsoport (-COOH)
A karboxilcsoport (-COOH) a szerves savak (karbonsavak) jellegzetes funkciós csoportja, amely a szénlánc végén található. Ez a csoport egy karbonil- és egy hidroxilcsoport kombinációjából áll, ami különösen erős savas tulajdonságokat kölcsönöz a molekulának. A karboxilcsoport jelenléte meghatározza a molekula oldhatóságát, forráspontját és sav-bázis tulajdonságait. A karbonsavak vízben jól oldódnak, mert a -COOH csoport hidrogénkötések létrehozására képes.
Éter- és észtercsoportok
Az étercsoport (-O-) két szénláncot köt össze egy oxigénatommal. Az észtercsoport (-COO-) egy karbonsav és egy alkohol reakciójából keletkezik. Az észterek szerkezete lehetővé teszi, hogy kellemes illatú és ízű vegyületek keletkezzenek, ezért az élelmiszeriparban aromaanyagként használják őket.
Aminocsoport (-NH₂) és amidcsoport
Az aminocsoport (-NH₂) egy vagy több szénatomhoz kapcsolódó nitrogénatom, amely bázikus tulajdonságokat ad a molekulának. Az aminok fontosak a gyógyszeriparban, valamint a fehérjék építőköveiként ismertek. Az amidcsoport különösen jelentős a fehérjék szerkezetének kialakításában, mivel a peptidek amidszerű kötésekkel kapcsolódnak egymáshoz.
Aromás gyűrűk
Az aromás gyűrű, például a benzolgyűrű, szénatomokból épül fel, amelyek delokalizált π-elektronokat tartalmaznak. Ez a szerkezet a szén különleges kötésképességének köszönhető, és rendkívül stabil molekulát eredményez. Az aromás funkciós csoportok, mint például a fenol (-OH aromás gyűrűhöz kötve), különleges fizikai és kémiai tulajdonságokkal bírnak.

A funkciós csoportok hatása a molekula tulajdonságaira
A funkciós csoportok döntő szerepet játszanak abban, hogy egy molekula milyen reakciókban vehet részt, milyen az oldhatósága, forráspontja, olvadáspontja, íze, illata, vagy akár biológiai aktivitása.
Fizikai tulajdonságok: Intermolekuláris kölcsönhatások
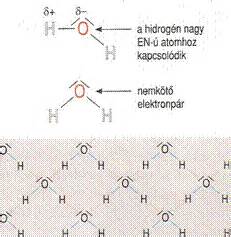
A funkciós csoportok befolyásolják az intermolekuláris kölcsönhatásokat, mint például a hidrogénkötés, a dipól-dipól kölcsönhatás és a Van der Waals-kölcsönhatás. Ezek a kölcsönhatások határozzák meg a vegyületek forráspontját, olvadáspontját és oldhatóságát. A hidroxilcsoport oxigénatomja nagy elektronegativitása miatt részlegesen negatív töltésű, a hidrogénatom pedig részlegesen pozitív töltésű. Az O-H kötés erősen poláris. A hidroxilcsoport jelenléte erős hidrogénkötések kialakulását teszi lehetővé, aminek hatására az alkoholok forráspontja jóval magasabb, mint az azonos szénatomszámú szénhidrogéneké. Az alkoholok forráspontja és olvadáspontja jelentősen magasabb, mint a hasonló molekulatömegű alkánoké vagy étereké. Ennek oka a molekulák közötti erős hidrogénkötések. Ahhoz, hogy az alkohol folyékony halmazállapotból gázneművé váljon (forrás), jelentős energiára van szükség ahhoz, hogy ezeket a hidrogénkötéseket felszakítsuk. Minél hosszabb az alkilcsoport (azaz minél nagyobb a molekulatömeg), annál nagyobb a van der Waals-erők szerepe is, ami tovább növeli a forráspontot.
Példa: Forráspontok összehasonlítása
| Vegyület | Molekulaképlet | Molekulatömeg (g/mol) | Forráspont (°C) |
|---|---|---|---|
| Etan | C₂H₆ | 30.07 | -88.6 |
| Dimetil-éter | CH₃OCH₃ | 46.07 | -24.8 |
| Etanol | C₂H₅OH | 46.07 | 78.3 |
Ez a táblázat jól illusztrálja, hogy az etanol, amelynek molekulatömege megegyezik a dimetil-éterével, de hidrogénkötéseket tud képezni, sokkal magasabb forrásponttal rendelkezik.
Az egyértékű alkoholok vízben való oldhatósága szintén a hidrogénkötéseknek köszönhető. A hidroxilcsoport képes hidrogénkötéseket kialakítani a vízmolekulákkal. Ahogy az alkilcsoport hossza növekszik, a molekula „szénhidrogénes” (nem poláris) része is növekszik. Ez a hidrofób rész egyre dominánsabbá válik, és gátolja a hidroxilcsoport és a víz közötti hidrogénkötés kialakulását. Ennek eredményeként a nagyobb molekulatömegű alkoholok oldhatósága vízben csökken. Az alkoholok sűrűsége általában kisebb, mint a vízé, bár ez a tendencia a molekulatömeg növekedésével változhat. A kisebb molekulatömegű alkoholok (C1-C11) szobahőmérsékleten folyékonyak. A tiszta alkoholok színtelenek. A kisebb molekulatömegű alkoholok jellegzetes, édeskés szagúak. A hidrogénkötések miatt az alkoholok viszkozitása nagyobb, mint a hasonló molekulatömegű alkánoké vagy étereké.
Kémiai tulajdonságok és reaktivitás: Elektronos és szterikus effektusok, sav-bázis viselkedés
A funkciós csoportok adják a molekula reaktív centrumát. Az alkoholok sav-bázis tulajdonságai is a hidroxilcsoportnak köszönhetőek. Az alkoholok nagyon gyenge savak, gyengébbek, mint a víz. Ennek ellenére képesek proton leadására, különösen erős bázisok, például alkálifémek vagy alkálifém-hidridek jelenlétében. Az alkoholátok erős bázisok, és gyakran használják őket szerves szintézisekben. Az alkoholok savassága függ az alkilcsoport szerkezetétől: a tercier alkoholok a legkevésbé savasak, a primer alkoholok a leginkább savasak. Az alkoholok a hidroxilcsoport oxigénatomján lévő nemkötő elektronpárok miatt gyenge bázisként is viselkedhetnek.
Az alkoholok oxidációja az egyik legfontosabb kémiai reakciójuk, amelynek termékei az alkohol típusától függenek. A primer alkoholok enyhe oxidációval aldehidekké (R-CHO) oxidálódnak. A szekunder alkoholok oxidációjával ketonok (R-CO-R’) keletkeznek. A tercier alkoholok nem rendelkeznek hidrogénatommal az -OH csoporthoz kapcsolódó szénatomon, ezért ellenállnak az oxidációnak anélkül, hogy a C-C kötések felszakadnának.
Az alkoholok vízelvonással alkénekké vagy éterekké alakíthatók, savas katalizátor (pl. kénsav) jelenlétében. Magasabb hőmérsékleten (pl. 170 °C) eliminációs reakcióval alkének keletkeznek, míg alacsonyabb hőmérsékleten (pl. 140 °C) kondenzációs reakcióval éterek képződhetnek. Az alkoholok karbonsavakkal vagy karbonsav-származékokkal (pl. savanhidridek, savkloridok) reagálva észtereket képeznek. Ez a reakció általában savas katalízis (pl. kénsav) hatására megy végbe. Például ecetsav és etanol reakciójával etil-acetát keletkezik.
Az alkoholok -OH csoportja gyenge távozó csoport, ezért közvetlenül nem reagálnak nukleofil szubsztitúcióval. Azonban protonálás után (R-OH₂⁺) a vízmolekula kiváló távozó csoporttá válik, így az alkoholok halogénsavakkal vagy más halogénezőszerekkel (pl. tionil-klorid) reagálva halogénezett szénhidrogéneket képeznek. A reakció mechanizmusa (SN1 vagy SN2) az alkohol típusától függ. Az alkoholok éghető anyagok, és megfelelő oxigénellátás mellett szén-dioxiddá és vízzé égnek el. Az alkoholok sokoldalú kémiai reaktivitása teszi őket rendkívül hasznos vegyületekké a szerves szintézisben és az iparban.
Az elektronos effektusok, mint az induktív és mezomer effektus, valamint a szterikus effektus mind hozzájárulnak a funkciós csoportok által meghatározott reaktivitáshoz. Az aktiváló csoportok, melyek benzolmolekulához kapcsolt funkciós csoportok, a benzolgyűrű elektronsűrűségét növelik, így az aromás elektrofilszubsztitúciós reakciók gyorsabban és könnyebben végbemennek a benzolmolekulán lejátszódó reakciókhoz képest. Az aktiváló csoportok relatív erősségüktől függően meghatározzák a benzolgyűrűn azokat a pozíciókat is, ahol a szubsztitúciós reakciók lejátszódnak. Az aktiváló csoportok által okozott elektronsűrűség-többlet főleg az orto- és para-helyzetű szénatomokon összpontosul, így nagyobb az esély, hogy a második csoportként belépő elektrofil ezeken a helyeken támad. A benzolszármazékokhoz kapcsolt aktiváló csoport erősségét három főbb tényező határozhatja meg: a mezomer effektus, az induktív effektus, és a hiperkonjugáció. E három közül a mezomer effektus a legmeghatározóbb jelenség. Így például a hidroxilcsoport (-OH) mezomer effektusból származó elektronküldő hatása erősebben érvényesül, mint az induktív effektusból adódó elektronszívó hatása. A nettó elektronküldő hatás miatt a hidroxilcsoport aktiváló hatású szubsztituens.
Izoméria és a funkciós csoportok
Az izoméria jelensége azt jelenti, hogy két vagy több vegyület azonos molekulaképlettel rendelkezik, de atomjaik eltérő térbeli elrendezése vagy kapcsolódási sorrendje miatt különböző szerkezettel és ebből adódóan eltérő tulajdonságokkal bírnak. A funkciós csoportok helyzete és jellege alapvetően meghatározza az izomerek típusait.
- Konstitúciós izomerek: Azok a molekulák, melyeknek eltérő az atomok kapcsolódási sorrendje.
- A láncizoméria akkor fordul elő, ha a szénlánc elágazásaiban van különbség.
- A helyzetizoméria akkor jelentkezik, ha a funkcionális csoport (jelen esetben az -OH csoport) különböző szénatomokhoz kapcsolódik a szénláncban.
- Az alkoholoknak lehetnek funkcionális csoport izomerei más vegyületosztályokkal. A leggyakoribb példa erre az éterek. Ezek a vegyületek drasztikusan eltérő fizikai és kémiai tulajdonságokkal rendelkeznek.
- Sztereoizoméria: Olyan izomériát jelent, ahol az atomok kapcsolódási sorrendje azonos, de térbeli elrendezésük eltér.
- Ha egy szénatomhoz négy különböző atom vagy atomcsoport kapcsolódik, akkor az a szénatom királis centrum (vagy aszimmetrikus szénatom).
- Az ilyen molekulák nem fedhetők le tükörképükkel, és két optikai izomer, úgynevezett enantiomer formájában léteznek.
- Például, a butan-2-ol királis centrumot tartalmaz a második szénatomján, mivel ahhoz egy hidrogénatom, egy hidroxilcsoport, egy metilcsoport és egy etilcsoport kapcsolódik.
Az izoméria kulcsfontosságú a szerves vegyületek sokféleségének megértésében. Az izoméria ismerete elengedhetetlen az alkoholok kémiai viselkedésének, fizikai tulajdonságainak és biológiai aktivitásának teljes megértéséhez.
The carbon cycle - Nathaniel Manning
Funkciós csoportok az iparban és a mindennapi életben
A funkciós csoportok alkalmazása elengedhetetlen a modern társadalomban. A háztartási vegyszerek, oldószerek, műanyagok, gyógyszerek, illatosítók, sőt még a textil és festékgyártás is mind a szén és funkciós csoportok kapcsolatára épülnek. Az iparban a funkciós csoportokat tartalmazó polimerek - például poliamidok vagy poliészterek - nélkülözhetetlenek a ruházati cikkek, csomagolóanyagok és műszaki eszközök gyártásában.
Az alkoholok a vegyipar egyik legfontosabb építőkövei. A metanol és az etanol különösen kiemelkedő ezen a téren. A metanolból formaldehid, ecetsav, metil-éter és számos más vegyület készül, amelyek a műanyagok, gyanták, ragasztók és gyógyszerek gyártásához elengedhetetlenek. Kiváló oldószerként való képességük miatt az alkoholok széles körben elterjedtek a festék- és lakkiparban, tintákban, ragasztókban és gyantákban.
Az alkoholok, különösen az etanol és a metanol, egyre nagyobb jelentőséggel bírnak az energiaszektorban, mint alternatív üzemanyagok. A bioetanol, amelyet biomasszából (kukorica, cukornád) állítanak elő, környezetbarát alternatívát kínál a fosszilis üzemanyagok kiváltására. A metanolt is kutatják és fejlesztik mint tiszta égésű üzemanyagot, különösen a hajózásban, ahol a szigorodó környezetvédelmi előírások miatt egyre nagyobb az igény az alacsonyabb károsanyag-kibocsátású megoldásokra. Az alkohol alapú üzemanyagok égése során kevesebb károsanyag (pl. korom) keletkezik.
Az etanol és az izopropil-alkohol nélkülözhetetlen az egészségügyben és a gyógyszeriparban. Fertőtlenítő és antiszeptikus tulajdonságaik miatt sebfertőtlenítőként, kézfertőtlenítő gélekben és felületfertőtlenítő szerekben használatosak. Az etanol számos gyógyszer oldószere is, és bizonyos gyógykészítményekben (pl. köhögéscsillapítókban) hatóanyagként is jelen van. A kozmetikai iparban az alkoholok széles körben alkalmazottak. Az etanol parfümök, dezodorok és hajlakok alapoldószere. Az izopropil-alkohol körömlakklemosókban és arcszeszekben fordul elő. A hosszú szénláncú zsíralkoholok (pl. cetil-alkohol) emulgeálószerként és bőrpuhítóként funkcionálnak krémekben és testápolókban. Az etanol az alkoholos italok alapvető összetevője. Emellett oldószerként használják élelmiszer-adalékanyagok, aromák és kivonatok előállításában. Az alkoholok sokfélesége és kémiai rugalmassága teszi őket az emberiség egyik legértékesebb vegyületcsoportjává.
Biztonsági megfontolások
Az egyértékű alkoholok széleskörű felhasználása ellenére elengedhetetlen a biztonságos kezelésük és a környezetvédelmi előírások betartása. Az alkoholok toxicitása nagymértékben függ a vegyület típusától és a bevitt mennyiségtől.
- Metanol: Ahogy már említettük, a metanol rendkívül mérgező. A szervezetben történő metabolizmusa során formaldehid és hangyasav keletkezik, amelyek súlyosan károsítják a látóideget, vakságot okozva, és metabolikus acidózishoz vezethetnek, ami halálos kimenetelű lehet.
- Etanol: Bár az etanol a szeszes italok hatóanyaga, túlzott fogyasztása akut alkoholmérgezést okozhat, amely eszméletvesztéssel, légzésdepresszióval és halállal járhat.
- Izopropil-alkohol: Az izopropil-alkohol kevésbé mérgező, mint a metanol, de lenyelése továbbra is veszélyes. Tünetei közé tartozik a hányinger, hányás, hasi fájdalom, szédülés, zavartság és a központi idegrendszer depressziója.
Az alkoholokkal való munkavégzés során mindig megfelelő egyéni védőeszközöket (pl. védőszemüveg, kesztyű) kell viselni, és gondoskodni kell a megfelelő szellőzésről. A legtöbb kis molekulatömegű alkohol gyúlékony folyadék. Gőzeik levegővel robbanóelegyet képezhetnek, ezért nyílt lángtól és gyújtóforrástól távol kell tartani őket, és megfelelő tárolási előírásokat kell betartani.

tags: #a #molekula #tulajdonsagait #dontoen #befolyasolo #atomcsoport





