A DNS-javítás mechanizmusai és jelentősége
A molekuláris sérülések strukturális károsodást okozhatnak a DNS-molekulában, és megváltoztathatják vagy megszüntethetik a sejt transzkripciós és génexpressziós képességét. Más léziók potenciálisan káros mutációkat indukálhatnak a sejt genomjában, amelyek befolyásolják a leánysejtek túlélését mitózis után. Következésképpen a DNS-javítás, mint a DNS-károsodási válasz (DDR) része, folyamatosan aktív.
A DNS-javítás mértéke egy sejten belül számos tényezőtől függ, beleértve a sejttípust, a sejt életkorát és a sejten kívüli környezetet. A sejt DNS-javító képessége létfontosságú a genom integritása szempontjából, és így a szervezet normális működése szempontjából.
A DNS-károsodás túlnyomó többsége az elsődleges kettős spirál szerkezetet érinti; vagyis maguk az alapegységek kémiailag módosulnak. Ezek a módosítások viszont megzavarhatják a molekulák szabályos spirál szerkezetét azáltal, hogy nem natív kémiai kötéseket vagy terjedelmes adduktokat hoznak létre, amelyek nem illeszkednek a standard kettős spirálba. A fehérjékkel és RNS-sel ellentétben a DNS általában hiányzik a harmadlagos szerkezetből, ezért ezen a szinten nem történik károsodás vagy zavar.
A sejtek osztódása előtti sérült DNS replikációja helytelen bázisok beépítéséhez vezethet a sérült bázisokkal szemben. A bázisok oxidációja [pl. A külső ágensek okozta károsodás sokféle formában jelentkezik. Az UV-A fény főként szabad gyököket hoz létre. Az ionizáló sugárzás, mint például a radioaktív bomlás vagy a kozmikus sugarak által létrehozott, a DNS-szálakban töréseket okoz. A magas hőmérsékleten fellépő termikus zavar növeli a depurinizáció (purin bázisok elvesztése a DNS gerincéről) és az egyszálú törések sebességét. Az UV-károsodás, alkiláció/metiláció, röntgensugárzás és oxidatív károsodás példák az indukált károsodásokra. A spontán károsodások közé tartozhat a bázis elvesztése, dezamináció, cukorgyűrű puckering és tautomer eltolódás.
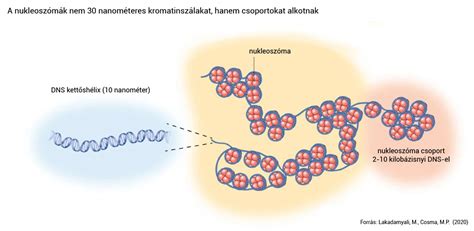
Az eukarióta sejtekben a DNS két sejthelyen található - a magban és a mitokondriumokban. A nukleáris DNS (nDNA) a sejtciklus nem replikatív szakaszaiban kromatin formájában létezik, és a sejtosztódás során kromo-szómáknak nevezett aggregált szerkezetekbe tömörül. Mindkét állapotban a DNS rendkívül kompakt, és hisztonoknak nevezett gyöngyszerű fehérjék köré tekeredik. Amikor egy sejtnek a kromoszómákban kódolt genetikai információt kell kifejeznie, a szükséges kromoszómaterület kibomlik, az ott található gének expresszálódnak, majd a terület visszatömörül nyugalmi konformációjába.
A mitokondriális DNS (mtDNA) a mitokondriumokon belül található, több példányban létezik, és számos fehérjéhez szorosan kapcsolódik, hogy nukleoidnak nevezett komplexet alkosson. A mitokondriumokon belül a reaktív oxigénfajok (ROS), vagy szabad gyökök, az adenozin-trifoszfát (ATP) folyamatos termelésének melléktermékei az oxidatív foszforiláción keresztül, erősen oxidatív környezetet teremtenek, amelyről ismert, hogy károsítja az mtDNA-t.
A szeneszcensia, egy irreverzibilis folyamat, amelyben a sejt már nem osztódik, a kromoszómavégek, az úgynevezett telomerek rövidülésére adott védő válasz. A telomerek ismétlődő nem kódoló DNS hosszú régiói, amelyek a kromoszómákat sapkaként fedik, és minden sejtosztódás során részlegesen leépülnek (lásd Hayflick-határ). Ezzel szemben a nyugalmi állapot a sejtes nyugalmi állapot reverzibilis állapota, amely nem kapcsolódik a genom károsodásához (lásd sejtciklus).
A szeneszcensia a sejtekben funkcionális alternatívája lehet az apoptózisnak olyan esetekben, amikor az organizmusnak térbeli okok miatt szüksége van egy sejt fizikai jelenlétére, ami "utolsó mentsvárként" szolgál a mechanizmus, amely megakadályozza, hogy a sérült DNS-sel rendelkező sejt helytelenül replikálódjon a pro-növekedési sejtes jelzés hiányában. A szabálytalan sejtosztódás daganat (lásd rák) kialakulásához vezethet, amely potenciálisan halálos az organizmusra nézve.
Fontos megkülönböztetni a DNS-károsodást és a mutációt, azaz a DNS-hibák két fő típusát. A DNS-károsodás és a mutáció alapvetően eltérő. A károsodás fizikai rendellenességeket eredményez a DNS-ben, például egyszálú és kétszálú töréseket, 8-hidroxideoxiguanozin reziduumokat és poliklikus aromás szénhidrogén adduktokat. A DNS-károsodást enzimek ismerhetik fel, és így helyesen javíthatók, ha rendelkezésre áll redundáns információ, például a komplementer DNS-szálon vagy egy homológ kromoszómán lévő sértetlen szekvencia a másoláshoz.
Ha egy sejt DNS-károsodást tart fenn, egy gén transzkripciója megakadályozható, és így a fehérjévé történő transzláció is blokkolódik. A DNS-károsodással ellentétben a mutáció a DNS bázisszekvenciájának megváltozása. A mutációt az enzimek nem tudják felismerni, amint a bázisváltozás mindkét DNS-szálban jelen van, és így a mutáció nem javítható. Sejtszinten a mutációk eltéréseket okozhatnak a fehérje funkciójában és szabályozásában. A mutációk replikálódnak, amikor a sejt replikálódik.
Tekintettel a DNS-károsodás és a mutáció ezen tulajdonságaira, látható, hogy a DNS-károsodás különleges probléma a nem osztódó vagy lassan osztódó sejtekben, ahol a nem javított károsodás idővel felhalmozódik. Másrészt, a gyorsan osztódó sejtekben a nem javított DNS-károsodás, amely nem öli meg a sejtet a replikáció blokkolásával, replikációs hibákat és így mutációkat fog okozni. A legtöbb nem semleges hatású mutáció káros a sejt túlélésére. Így az osztódó sejtekből álló szövetet alkotó sejtek populációjában a mutáns sejtek általában elvesznek. Azonban a ritka mutációk, amelyek túlélési előnyt biztosítanak, hajlamosak klonálisan terjedni a szövetben lévő szomszédos sejtek rovására. Ez az előny a sejt számára hátrányos az egész organizmusra nézve, mert az ilyen mutáns sejtek rákot okozhatnak. Így a gyakran osztódó sejtekben előforduló DNS-károsodás, mivel mutációkat eredményez, a rák egyik kiemelkedő oka.
A sejtek nem tudnak működni, ha a DNS-károsodás rontja a genom alapvető információinak integritását és hozzáférhetőségét (de a sejtek felszínesen funkcionálisak maradnak, ha nem alapvető fontosságú gének hiányoznak vagy sérültek). A DNS kettős spirál szerkezetében okozott károsodás típusától függően számos javítási stratégia fejlődött ki az elveszett információ helyreállítására. Ha lehetséges, a sejtek a DNS komplementer szálát vagy a testvérkromatidot használják sablonként az eredeti információ helyreállítására. A DNS károsodása megváltoztatja a spirál térbeli konfigurációját, és ezeket a változásokat a sejt érzékeli.
Ismeretes, hogy a sejtek kémiailag visszafordítva háromféle károsodást küszöbölnek ki DNS-ükben. Ezek a mechanizmusok nem igényelnek sablont, mivel az általuk ellensúlyozott károsodástípusok csak az négy bázis egyikében fordulhatnak elő. Az ilyen közvetlen reverziós mechanizmusok specifikusak a károsodás típusára, és nem járnak a foszfodieszter gerinc törésével. Az UV-fény által okozott pirimidin dimerek képződése rendellenes kovalens kötést eredményez a szomszédos pirimidin bázisok között. Egy másik károsodási típus, a guanin bázisok metilációja közvetlenül megfordítható a metil guanin metil transzferáz (MGMT) enzim által, amelynek bakteriális megfelelője ogt.
Bázis-exíziós javítás (BER): A sérült egyszálú bázisokat vagy nukleotidokat leggyakrabban a bázis vagy az érintett nukleotid eltávolításával, majd a helyes bázis vagy nukleotid beillesztésével javítják. A bázis-exíziós javítás során egy glikoziláz enzim eltávolítja a sérült bázist a DNS-ből, megrepesztve a bázis és a dezoxiribóz közötti kötést. Ezek az enzimek egyetlen bázist távolítanak el, hogy apurinikus vagy apyrimidinikus helyet (AP helyet) hozzanak létre. AP endonukleázoknak nevezett enzimek az AP helyen megrepesztik a sérült DNS-gerincet.
Nukleotid-exíziós javítás (NER): A terjedelmes, spirált torzító károsodásokat, mint például az UV-fény által okozott pirimidin dimerek, általában egy háromlépéses folyamat javítja.
Hibajavító rendszerek: A hibajavító rendszerek lényegében minden sejtben jelen vannak, hogy kijavítsák azokat a hibákat, amelyeket az ellenőrző leolvasás nem javít meg. Ezek a rendszerek legalább két fehérjéből állnak. Az egyik érzékeli a hibát, a másik pedig egy endonukleázt toboroz, amely a sérült régió közelében megrepeszti az újonnan szintéziselt DNS-szálat. Az E. coli-ban az érintett fehérjék a Mut osztályú fehérjék: MutS, MutL és MutH. A legtöbb eukariótában a MutS analógja az MSH, a MutL analógja pedig az MLH. A MutH csak baktériumokban található meg.
Kettős szálú törések javítása: A kettős szálú törések, amelyekben a kettős spirál mindkét szálát átvágják, különösen veszélyesek a sejtre nézve, mivel genomátrendeződésekhez vezethetnek.
Nem-homológ végek összekapcsolása (NHEJ): Az NHEJ-ben a DNS-ligáz IV, egy speciális DNS-ligáz, amely komplexet alkot az XRCC4 kofaktorral, közvetlenül összekapcsolja a két véget. A pontos javítás irányításához az NHEJ rövid homológ szekvenciákra támaszkodik, amelyeket mikrohomológiáknak neveznek, és amelyek a csatolandó DNS-végek egyszálú farkain találhatók. Ha ezek a túlnyúlások kompatibilisek, a javítás általában pontos. Az NHEJ a javítás során mutációkat is bevezethet. A törési helyen lévő sérült nukleotidok elvesztése deléciókhoz vezethet, a nem egyező végek összekapcsolása pedig inszerciókat vagy transzlokációkat hoz létre. Az NHEJ különösen fontos a sejt DNS-ének replikációja előtt, mivel nincs sablon a homológ rekombinációval történő javításhoz.
Mikrohomológia-közvetített exíziós javítás (MMEJ): Az MMEJ rövid távú végek exíziójával kezdődik egy kettős szálú törés mindkét oldalán az MRE11 nukleáz által a mikrohomológia régiók feltárása érdekében. További lépésekben szükség van a polí (ADP-ribóz) polimeráz 1 (PARP1) enzimre, amely az MMEJ korai lépése lehet. A mikrohomológia régiók párosítása, majd a flap szerkezet-specifikus endonukleáz 1 (FEN1) toborzása a túlnyúló flapek eltávolítására történik. Ezt követi az XRCC1-LIG3 toborzása a helyszínre a DNS-végek ligálásához, ami egy intakt DNS-hez vezet.
Homológ rekombináció (HR): A HR megköveteli egy azonos vagy csaknem azonos szekvencia jelenlétét, amelyet sablonként használnak a törés javításához. A folyamatért felelős enzimatikus gépezet szinte azonos a meiózis során a kromoszómális kereszteződésért felelős gépezettel. Ez az út lehetővé teszi egy sérült kromoszóma javítását egy testvérkromatid (DNS replikáció után a G2-ben elérhető) vagy egy homológ kromoszóma sablonként való felhasználásával.

A Deinococcus radiodurans extremofil baktérium csodálatos képességgel rendelkezik az ionizáló sugárzás és más források okozta DNS-károsodás túlélésére. Legalább két példányban a genom, véletlenszerű DNS-törésekkel, DNS-fragmentumokat képezhet anneálással. Azrészlegesen átfedő fragmentumokat homológ régiók szintézisére használják egy mozgó D-hurok révén, amely addig folytathatja a kiterjedést, amíg komplementer partner szálakat találnak.
A topozomerázok egyszálú és kettős szálú töréseket is bevezetnek a DNS szuperkötöttségi állapotának megváltoztatása során, ami különösen gyakori a nyitott replikációs villa közelében. A DNS kettős szálú töréseinek egy másik típusa a hőérzékeny vagy hőstabil DNS-helyekből származik. Ezek a DNS-helyek nem kezdeti DSB-k. Azonban magas hőmérsékleten történő kezelés után DSB-kké alakulnak. Az ionizáló sugárzás rendkívül összetett DNS-károsodást okozhat, mint a klaszterezett károsodás. Ez különböző típusú DNS-léziókat tartalmaz a DNS-spirál különböző helyein. Ezen közel elhelyezkedő léziók közül néhány valószínűleg DSB-kké alakul magas hőmérsékletnek kitéve.
Transzléziós szintézis (TLS): A transzléziós szintézis (TLS) egy DNS-károsodás-tolerancia folyamat, amely lehetővé teszi a DNS-replikációs gépezet számára, hogy át tudjon mászni a DNS-léziókon, például timin dimereken vagy AP helyeken. Ez magában foglalja a rendes DNS-polimerázok speciális transzléziós polimerázokra (pl. Y polimeráz családba tartozó DNS-polimeráz IV vagy V) való cseréjét, amelyek gyakran nagyobb aktív helyekkel rendelkeznek, amelyek elősegíthetik a bázisok beillesztését sérült nukleotidokkal szemben. A polimeráz cserét a replikációs folyamatosságot biztosító PCNA poszttranszlációs módosítása, többek között, közvetíti. A transzléziós szintézis polimerázok gyakran alacsony hűségűek (magas arányban helytelen bázisokat illesztenek be) az ép mintákkal szemben a rendes polimerázokhoz képest. Azonban sokuk rendkívül hatékony a helyes bázisok beillesztésében specifikus károsodástípusokkal szemben. Például a Pol η hiba-mentes átjutást tesz lehetővé az UV-sugárzás által indukált léziók felett, míg a Pol ι mutációkat okoz ezeken a helyeken. A Pol η az első adenin beillesztését végzi a T^T fotodimerrel szemben Watson-Crick bázispárosítással, a második adenint pedig szin konformációban illeszti be Hoogsteen bázispárosítással.
Sejtszinten a transzléziós szintézis során bekövetkező pontmutációk kockáztatása előnyösebb lehet, mint a drasztikusabb DNS-javítási mechanizmusokhoz folyamodni, amelyek súlyos kromoszómális aberrációkat vagy sejthalált okozhatnak. Röviden, a folyamat speciális polimerázokat foglal magában, amelyek vagy megkerülik, vagy javítják a léziókat a megállt DNS-replikáció helyein. Például az emberi DNS-polimeráz eta képes megkerülni a komplex DNS-léziókat, mint a guanin-timin intra-strand keresztkötés, G[8,5-Me]T, bár célzott és félig célzott mutációkat okozhat. Paromita Raychaudhury és Ashis Basu tanulmányozták ugyanezen lézió toxicitását és mutagenezisét Escherichia coli-ban, replikálva egy G[8,5-Me]T-módosított plazmidot E. coli-ban specifikus DNS-polimeráz knockoutokkal. A proliferáló sejtmagi antigén (PCNA) biztosítja a platformot ezeknek a polimerázoknak a megkerüléshez. Normál körülmények között a polimerázokhoz kötött PCNA replikálja a DNS-t. A lézió helyén a PCNA-t a RAD6/RAD18 fehérjék ubikvitinálják vagy módosítják, hogy platformot biztosítsanak a speciális polimerázok számára a lézió megkerüléséhez és a DNS-replikáció folytatásához. A transzléziós szintézis után kiterjesztés szükséges. Ezt a kiterjesztést egy replikatív polimeráz végezheti el, ha a TLS hiba-mentes, mint a Pol η esetében, de ha a TLS hibás párosítást eredményez, akkor egy speciális polimerázra van szükség a kiterjesztéshez; Pol ζ. A Pol ζ abban egyedi, hogy képes kiterjeszteni a terminális hibás párosításokat, míg a jobban processzív polimerázok nem képesek rá.
Az ionizáló sugárzásnak, ultraibolya fénynek vagy vegyszereknek kitett sejtek hajlamosak több, terjedelmes DNS-lézió és kettős szálú törés helyének megszerzésére. Ezenkívül a DNS-károsító ágensek más biomolekulákat is károsíthatnak, például fehérjéket, szénhidrátokat, lipideket és RNS-t. A károsodás felhalmozódása, pontosabban a replikációs villákat megakasztó kettős szálú törések vagy adduktok, ismertek a globális DNS-károsodási válasz stimuláló jelei közé tartoznak. A károsodásra adott globális válasz a sejtek saját megőrzésére irányuló cselekedet, és elindít számos makromolekuláris javítási, lézió megkerülési, tolerálási vagy apoptózisos útvonalat.
Az eukarióta DNS kromatinba csomagolása akadályt jelent minden DNS-alapú folyamat számára, amelyek enzim toborzást igényelnek a hatás helyére. A DNS-javítás lehetővé tételéhez a kromatin át kell alakuljon. A kromatin lazulása gyorsan bekövetkezik a si...
A sok teszt törzs közül sok rendelkezik olyan jellemzőkkel, amelyek érzékenyebbé teszik őket a mutációk kimutatására, beleértve a reverziós helyek DNS-szekvenciáit, a megnövekedett sejtpermeabilitást nagy molekulák iránt, valamint a DNS-javító rendszerek kiiktatását vagy a hibára hajlamos DNS-javítási folyamatok fokozását.
Az emlős májsejtekkel végzett nem ütemezett DNS-szintézis (UDS) in vivo vizsgálat célja azon anyagok meghatározása, amelyek DNS-reparációt váltanak ki a kezelt állatok májsejtjeiben.
Nem ütemezett DNS-szintézis (UDS): Reparációs DNS-szintézis, miután egy kémiai anyagok vagy fizikai ágensek által indukált károsodási régiót tartalmazó DNS-szakasz kivágódott és eltávolítódott.
A bakteriális reverz mutációs teszt prokarióta sejteket használ, amelyek az olyan tényezőkben térnek el az emlőssejtektől, mint például a kémiai anyagok felvétele, metabolizmus, kromoszóma szerkezet és DNS-javítási folyamatok.
Ez az in vivo emlős mikronukleusz teszt különösen releváns a mutagén veszély felmérésében, mivel lehetővé teszi az in vivo metabolizmus, farmakokinetika és DNS-javítási folyamatok tényezőinek figyelembevételét, bár ezek eltérőek lehetnek a fajok, a szövetek és a genetikai végpontok között.
A keresztkötés mutagének kimutatása érdekében előnyösebb lehet a TA102 törzs bevonása, vagy egy DNS-javításra képes E. coli törzs (pl. E. coli WP2 vagy E. coli WP2 (pKM101)) hozzáadása.
A vizsgált végpont következtetni enged a májsejtekben a DNS-károsodásra és az azt követő reparációra.
Ezenkívül mutagén hatások jöhetnek létre DNS-elváltozások helyre nem állítása, nem megfelelő helyreállítása vagy hibás replikációja miatt.
Mi történik, ha a DNS-ed megsérül? - Monica Menesini
A kutatócsoport úttörő munkát végzett azzal, hogy DNS-javító géneket túltermelő Drosophila törzseket hozott létre, és ezeket sikeresen kijuttatta a Nemzetközi Űrállomásra az AX-4 misszió keretében. A projekt másik részében ugyanezeket a géneket humán sejtekben is túltermeltették, majd sugárkezelést követően elemezték a sejtek DNS-ében kialakuló kettős szálú töréseket. A projekt megvalósítása három kutatócsoport szoros együttműködésével valósult meg.
A kozmikus sugárzás az emberi űrutazások egyik legnagyobb kihívása. A Föld természetes védelme nélkül az űrhajósokat jóval erősebb, a DNS-t is károsító részecskék érik, amelyek hosszú távon komoly egészségügyi kockázatot jelentenek.
A sejtjeink genomjának integritását vizsgáló laboratóriumunk genetikai, biokémiai és proteomikai megközelítéseket használva fejti fel a molekuláris mechanizmusokat a betegségek jobb megértése érdekében. Célunk a sejtjeinken belüli genom integritás fenntartásának alapvető folyamatainak jobb megértése.
Figyelemre méltó, hogy genomunkban kódolt információ hogyan őrződik meg páratlan precizitással, ugyanakkor elég rugalmas ahhoz, hogy képes legyen alkalmazkodni a környezeti változásokhoz. A DNS-javítási folyamatok a biológia kulcsfontosságú aspektusai, mivel e mechanizmusok helytelen szabályozása gyakran számos ráktípus és neurodegeneratív betegség hajtóereje. Ezen betegségek alapjául szolgáló molekuláris mechanizmusok feltárásával célunk új terápiás megközelítések alapjainak megteremtése.
Az idegi DNS-javítás molekuláris mechanizmusai: Az idegrendszeri rendellenességek a rokkantság és a halálozás egyik vezető okai világszerte. Célunk az idegsejtek DNS-javításában bekövetkező hibák jobb megértése, és e tudás kihasználása a neurodegenerációban rejlő új sebezhetőségek azonosítására. Az idegrendszer rendkívül érzékeny minden típusú stresszre, beleértve a DNS-károsodást is, nagy energiaigénye, magas transzkripciós aktivitása és e sejtek hosszú élettartama miatt. Az adatok arra utalnak, hogy a DNS-javító génekben lévő mutációk számos neurológiai rendellenességgel és szomatikus tri/dinukleotid expanzióval társulnak, amelyek kritikus szerepet játszanak a neurodegeneratív betegségek, mint a Huntington-kór (HD) vagy az amiotrófiás laterális szklerózis (ALS) kialakulásában. Az idegsejtek fiziológiás körülmények között képesek javítani és védeni genomjukat a DNS-károsodástól, annak ellenére, hogy hiányzik a DNS-replikáció, ami korlátozza a DNS-javításra való lehetőségüket.
Inhibitor szűrés és tervezés: Célunk, hogy kis molekulájú inhibitorokat azonosítsunk releváns exonukleázok ellen, hogy segítsük a meglévő onkológiai terápiákat. Egy új, nagy áteresztőképességű aktivitás teszt segítségével célunk kis molekulájú inhibitorok azonosítása az onkológiai immunterápia szempontjából releváns exonukleázok számára.
A transzléziós DNS-polimerázok funkciói: Minden sejtünknek naponta több tízezer DNS-lézióval kell megbirkóznia. A léziók pontos természetétől és a sejtciklus fázisától függően a javítást a DNS-javítási útvonalak egyikének kell elvégeznie. A sejtek különleges kihívással néznek szembe, amikor DNS-léziót tapasztalnak, akár az S-fázisban végzett DNS-replikáció, akár a DNS-javítási szintézis (amely a DNS-javítási folyamat réskitöltő lépése) során. A DNS-elongációs folyamatok során használt replikatív DNS-polimerázok katalitikus helye kompakt, és nem képes befogadni a legtöbb DNS-léziót. Következésképpen a DNS-szintézis a legtöbb DNS-lézió formájánál megáll. Ekkor indul el egy polimerázcsere a PCNA-n, ahol a replikatív DNS-polimerázot transzléziós polimerázok váltják fel, hogy megkerüljék ezeket a léziókat. Ezt a folyamatot transzléziós szintézisnek (TLS) nevezik.
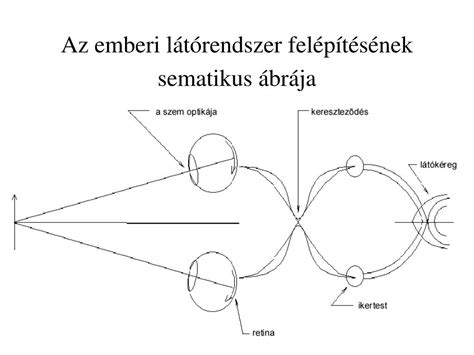
A DNS-javítási folyamatok létfontosságúak a genom integritásának megőrzésében, mivel ezek hiánya vagy hibás működése számos betegség, köztük a rák és a neurodegeneratív rendellenességek kialakulásához vezethet.
tags: #dna #repair #foci #jelentese





